近頃CMなどでよく耳にする「機能性表示食品」とは何か?
特定保健用食品(トクホ)や栄養機能食品とは何が違うのか?
をわかりやすくまとめました。
「機能性表示食品」の届出を検討している企業担当者様もぜひご覧ください。
機能性表示食品とは?
能性表示食品とは「おなかの調子を整えます」「脂肪の吸収をおだやかにします」など、健康の維持及び増進に役立つという食品の機能性(効果)を商品パッケージに表示できる、サプリメント、加工食品、生鮮食品を含めた、すべての食品のことです。(一部除く)
安全性の確保と科学的根拠(エビデンス)を前提に消費者庁に届け出し、事業者の責任のもと表示され、消費者である私たちが誤認することなく商品を選択できるよう、適正な表示などによる情報提供が行われます。

機能性が表示されている食品
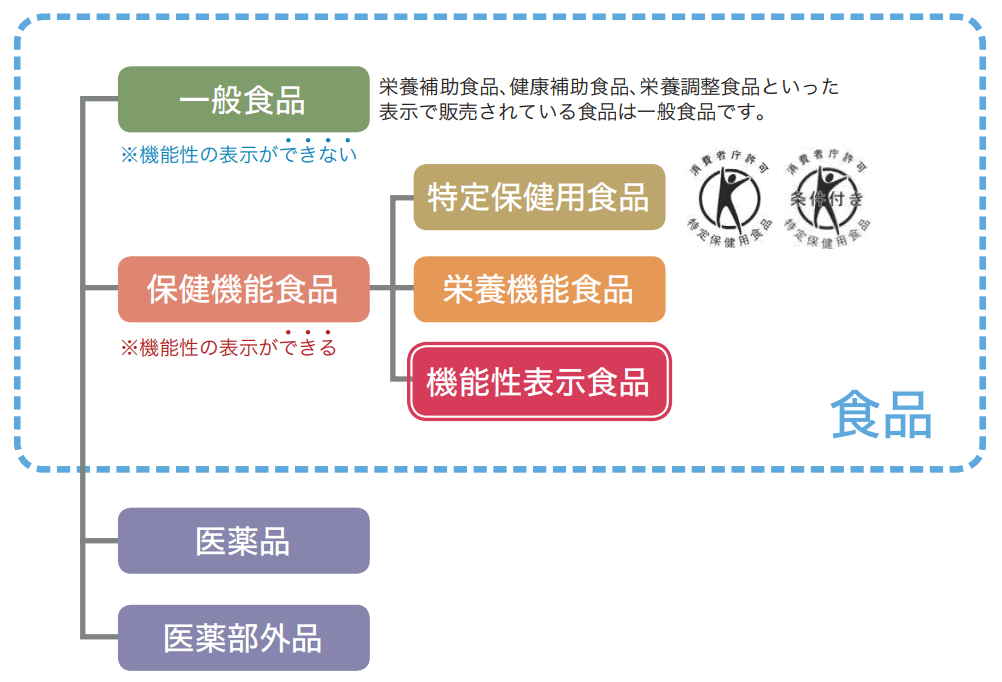
実は機能性表示食品が導入以外にも、機能性を表示できる食品区分が従来からありました。
これらの制度を総称して「保健機能食品制度」と言い、「機能性表示食品」の他にみなさんおなじみの「特定保健用食品(トクホ)」と「栄養機能食品」という区分が認められています。
特定保健用食品(トクホ)

栄養機能食品
国が定めた特定の栄養成分(ビタミン、ミネラルなど)の摂取目安量に適合した食品です。
一日に必要な栄養成分が不足しがちな場合、その補給・補完のために利用できます。

機能性表示食品
事業者の責任で、科学的根拠を基に商品パッケージに機能性を表示するものとして、消費者庁に届け出られた食品が機能性表示食品です。
機能性表示食品では「おなかの調子を整えます」「脂肪の吸収をおだやかにします」など、特定の保健の目的が期待できる(健康の維持及び増進に役立つ)という食品の機能性を表示することができます。
参考資料:消費者庁「「機能性表示食品」って何?」
以下にそれぞれの区分のメリット/デメリットを踏まえた比較表をまとめました。
保健機能食品比較表
安全性の確保と科学的根拠を前提に消費者庁に届出(届出のみ) | マークなし、パッケージに「機能性表示食品」と表示されている | 事業者の責任において機能性(効果)を表示できる | ||
(トクホ) | 機能性(効果)や安全性を個別審査 | 食品ごとに消費者庁長官が許可 | 消費者庁許可のマークがあり、「特定保健用食品」と表示されている | 許可手続きに時間と費用がかかる |
許可・届出は不要 | マーク無し | 国が定めた表現によって機能性(効果)を表示 / 対象成分が限定されている |
食品と医薬品の分類表

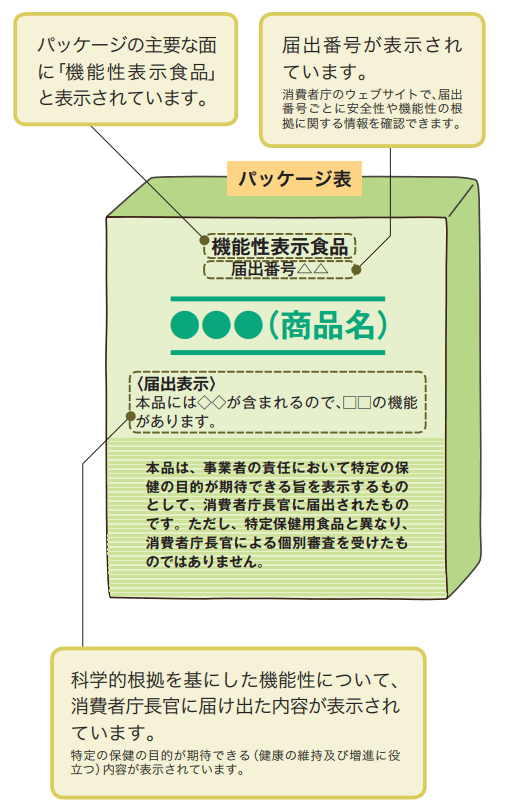
機能性表示食品の表示例
<パッケージ表>
- 機能性表示食品である旨
- 届出番号
- 消費者庁長官に届け出た機能性
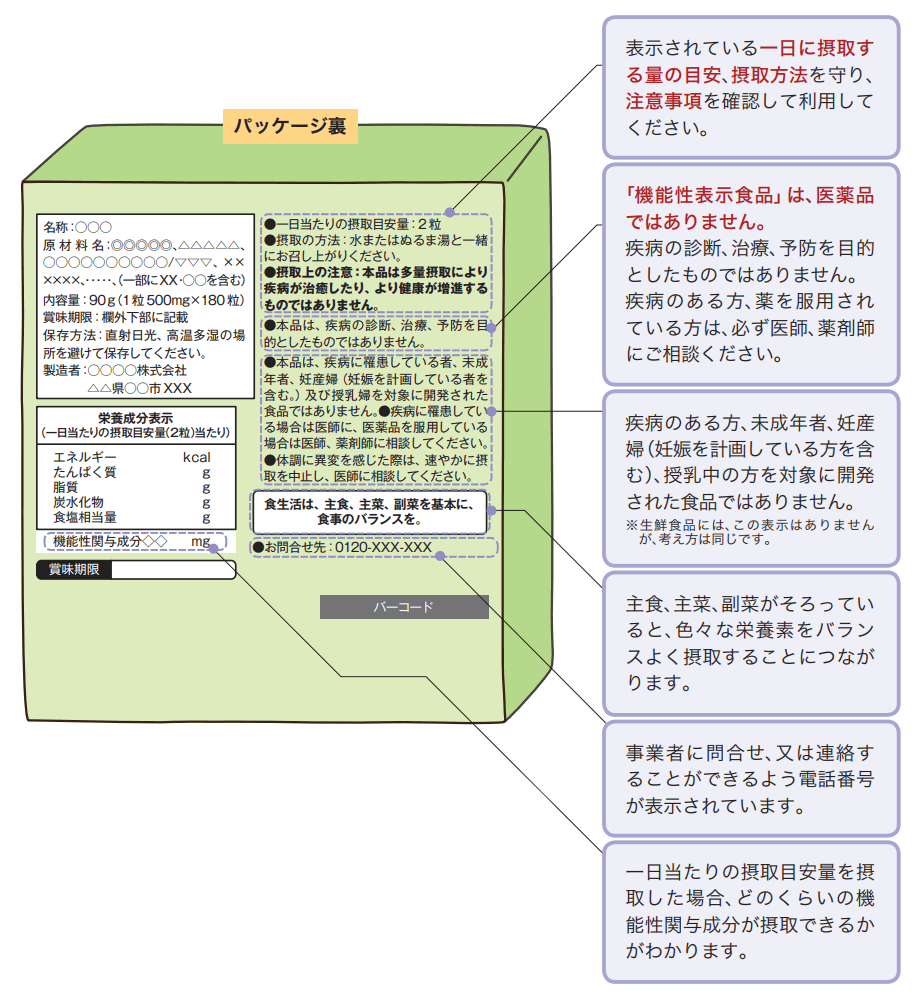
<パッケージ裏>
- 1日当たりの摂取目安量
- 摂取方法
- 注意事項
- 医薬品ではない旨
- 疾病の罹患者、未成年者、妊産婦(妊娠を計画している方を含む)および授乳婦を対象に開発された食品ではない旨
- 「食生活は、主食、主菜、副菜を基本に、 食事のバランスを。」という食事のバランスに関する記述
- 事業者の連絡先
- 1日当たりの摂取目安量当たりの機能性関与成分の含有量
最終的に、これらの届け出情報は消費者庁のウェブサイトで公開され、消費者は安全性や機能性がどのように確保されているのか、データベース一覧で確認できます。

機能性表示ができない食品
- アルコールを含む飲料、塩分・糖分・脂質等の過剰摂取につながる食品
- 「専ら医薬品として使用される成分本質(原材料)リスト」に指定された成分を含んだ食品
- 特別用途食品(病気の方、乳幼児、高齢者など、通常の食事を食べることが出来ない人のための特別な用途を目的とした食品)
- 食事摂取基準に基準が策定されている栄養素を含んだ食品
- 病気の罹患者、未成年、妊産婦(妊娠を計画している方を含む)および授乳婦を対象とした食品

機能性表示食品で「認められる表現」と「認められない表現」

| 容易に測定可能な体調の指標の維持に適する または改善に役立つな どの表現 | 「血圧が高めの方に」 「体に脂肪がつきにくい」 「中性脂肪を低下させる」 など |
|
身体の生理機能、組織機能の良好な維持に適する または改善に役立つなどの表現 | 「目のピント調節機能改善」 「目の疲労感の緩和」 「糖の吸収を抑えます」 など |
|
身体状態を本人が自覚でき、 一時的な体調の変化(継続的、慢性的でないもの) の改善に役立つなどの表現 | 「一時的なストレスの低減」 「一時的な疲労感の緩和」 「VDT作業時の一時的な目の不快感」 など |
|
| 病気の予防・診断・治療効果を暗示する表現 | 「糖尿病の疑いがあるあなたへ」 「花粉症が治ります」 「風邪の予防に」 など |
|
健康の維持・増進の範囲を超えた、 意図的な健康の増強を主張する表現 |
機能性表示食品とトクホの違い
共に「健康の維持及び増進に役立つ」という食品の機能性について表示するトクホと機能性表示食品ですが、その制度の違いは具体的にどのようなことが挙げられるのか、ここからは詳しく説明いたします。
機能性表示食品のメリットは「早く」て「広い」
機能性表示食品と特定保健用食品(トクホ)の違いについては「わかりにくい」という声が聞かれますが、機能性表示食品の特徴を一言で言えば、下記の通りです。
- 取得までの所要時間:早い
- 対象となるヘルスクレーム:広い
もう少しポイントを絞って解説します。
国の審査
機能性(効果)や安全性を個別に審査 |
健康食品は、薬機法の規制により、効果効能をうたえませんが、機能性表示食品と特定保健用食品(トクホ)ともに、要件をクリアすると、一定の効果(機能性)をうたうことができる制度です。
一見、似たような制度ですが、機能性表示食品が事業者の責任で届出するのに対し、特定保健用食品(トクホ)は許可型である点、審査の違いがあります。
手続・承認
(トクホ) |
|
|---|---|
食品ごとに消費者庁長官が許可 | 安全性の確保と科学的根拠を前提に消費者庁に届出(届出のみ) |
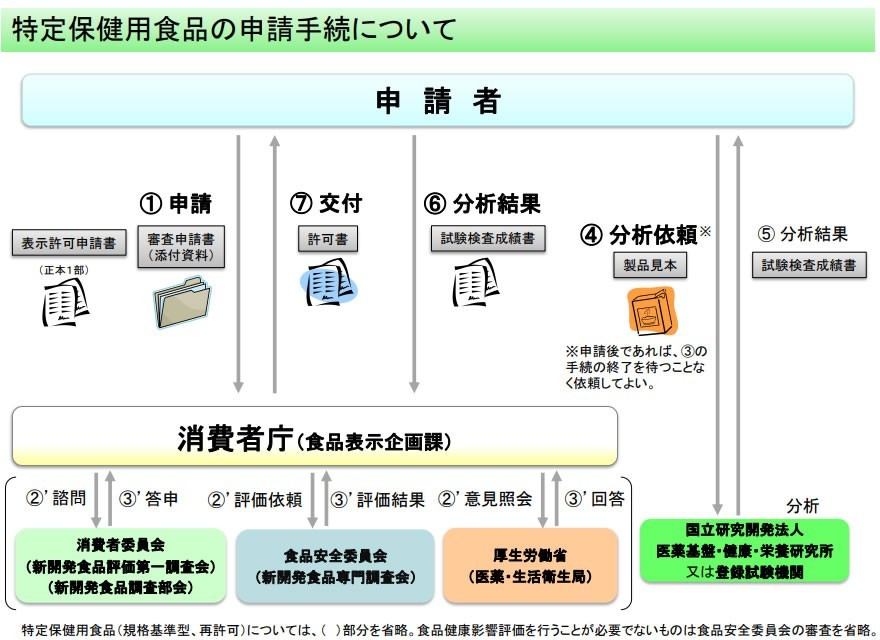
特定保健用食品(トクホ)の場合、企業は営業所所在地の都道府県知事を通じて表示許可申請書と審査申請書を消費者庁(食品表示企画課)に提出し、消費者庁が消費者委員会・食品安全委員会・厚生労働省と連携して審査を行います。
審査において食品の 安全性と効果が認められれば 、国立健康・栄養研究所(または登録試験機関)でのサンプル分析を経て、消費者庁が特定保健用食品として許可します。
(出典:消費者庁)
特定保健用食品(トクホ)は、商品ごとに安全性試験・有効性試験を求められるなど手続コストや時間の負担が大きくなるため今まで中小企業にとってはハードルの高い制度でした。
そのため新しくできた機能性表示食品という制度は中小企業にとって格段に使い勝手の良い制度と言えるでしょう。
こうした審査・手続・承認上の違いから、浸透するスピードに大きな違いが見られます。
ヘルスクレーム
(トクホ) |
|
|---|---|
機能性表示食品は、認められるヘルスクレームが広く、特定保健用食品(トクホ)にはない生鮮食品の届出も認められています。
事実、両者の届出数を比較すると、大きな開きがあります。
特定保健用食品(トクホ): 1991年にスタート
→承認された商品1,074品目(2020年3月末)
機能性表示食品: 2015年にスタート
→届出件数は3,722件
今後、ますます機能性表示食品優位の傾向は強まるでしょう。
ただし、名目上は国の審査がない機能性表示食品ですが、厳しい書類審査があり、事実上「許可」制に近い状態です。
一度受理された商品も、後日、調査を経て、不備を指摘されると書類の追加提出や撤回を求められることがある点、注意が必要です。
機能性表示食品が生まれた背景

機能性表示食品は、アメリカの同様の制度にならい、2015年(平成27年)4月から導入されました。
元々、日本では健康食品の機能性や効果効能表現に強い規制がかけられていました。 医薬品ではないため、医薬品的な効能効果を標榜すると「無承認の医薬品の販売」として、薬機法違反とみなされていたのです。
一方で「朝からスッキリ」「新聞の細かい字が気にならない」といった抽象的で暗示的な表現では、正しい判断をするのは難しいですよね。
そこで消費者が、商品の特徴を誤認することなく自主的かつ合理的に商品を選択できるよう、一定の要件を満たせば、適正な表示による情報提供を認めたのがこの制度なのです。
機能性を表示するための3つのルール
- 安全性の確保
└十分な食経験があること - 機能性の担保
└機能性の化学的証拠(エビデンス)の明確化(臨床試験・研究レビュー) - 適正な表示による消費者への情報提供
└消費者に誤解を与えない情報の表示になっているか
機能性表示食品の対象と要件
機能性を表示するための必要事項
- 安全性の評価
- 機能性の評価
└RCT(Randomized Controlled Trial ):最終製品を用いたヒトの臨床試験
└SR(Systematic Review):最終製品または機能性関与成分に関する研究レビュー - 生産・製造、品質の管理体制
- 健康被害の情報収集体制

RCTのみを要件とする特定保健用食品(トクホ)と異なり、SRでも機能性を表示できるのが大きなメリットです。
研究レビューとは



機能性表示食品の届出の流れ
パッケージ記載事項としてどのような機能性を表示するのかを決め、エビデンスと共に、消費者庁に届け出
届出を得た消費者庁は書類を調べて問題なければ受理番号を交付し、その届出を消費者庁HPに反映
消費者庁HPに反映し、60日間経過の後、特に問題が出なければ販売スタート(販売前届出制度)
パッケージ記載事項としてどのような機能性を表示するのかを決め、エビデンス(機能性エビデンス、成分エビデンス)と共に、消費者庁に届け出ます。
届出を得た消費者庁は書類を調べて問題なければ受理番号を交付し、その届出を消費者庁HPに反映します。
消費者庁HPに反映し、60日間経過の後、特に問題が出なければ販売スタートできます(販売前届出制度)。
なお、エビデンスづくりで最も時間がかかるのは前述したヒトの臨床試験。
最大12週間要する上、試験結果を論文にまとめ査読つき雑誌に掲載しなければなりませんので、トータル半年ほどかかります。
従って、機能性表示の実施を意思決定してから販売できるまで最低9~10ヶ月ほど見ておいた方がよさそうです。
機能性表示食品の落とし穴
無事、機能性表示食品の届出を受理されたとしても、それだけで商品は売れません。 広告やサイト、LP(ランディングページ)を通じて消費者に魅力訴求する必要があるでしょう。
この時、誇大表現をするとどうなるでしょう?
せっかく機能性や効果効能表現をうたえても、今度は健康増進法や景品表示法に触れる可能性があるのです。
ニュースでもよく、措置命令や課徴金納付命令を下された企業が報道されますが、レピュテーションリスクや経済的損害など、事業運営に多大な影響を及ぼします。
機能性表示食品で困ったら、薬事法ドットコムへ
薬機法の広告規制により、魅力を十分に伝えられなかった商品も、機能性表示食品を取得すれば「おなかの調子を整えます」「脂肪の吸収をおだやかにします」などの効果効能(機能性)をうたうことができます。
一方で、前述したように、機能性表示食品にも「認められる表現」「認められない表現」があることは意外に知られていません。
結果、リサーチや準備不足のまま届出し、何度も差し戻しされ、前に進まないというケースが散見されます。
薬機法と薬事行政を知り尽くし、日本一の機能性表示関与実績を誇る薬事法ドットコムなら、こうしたお悩みにも対応可能です。スムーズな届出と貴社の売上アップにつながる訴求を実現いたします。
弊社は国内最高峰の薬事コンサルティング企業として、高級官僚OB(大蔵省・厚生省・警察庁)、元検事長・政府委員など、法律・行政・医学・統計学・マーケティングの権威が集結し、最新の動向を踏まえ、マーケティング効果と法令遵守のバランスを第一に考えたコンサルティングを提供いたします。