2015年の制度開始以来、拡大を続ける機能性表示食品の市場。その機能性表示食品の市場動向をレポートとしてまとめました。本記事では、2023年までの届出件数や人気の成分・機能性などのランキングをご紹介。そのほか、「さくらフォレスト事件」など2023年の機能性表示食品の業界における注目トピックや最新トレンド、今後必要となる対策も解説します。
1. 機能性表示食品の届出件数は7000件突破!市場拡大が続く
機能性表示食品とは「おなかの調子を整えます」「脂肪の吸収をおだやかにします」など、健康の維持・増進に役立つ食品の機能性(効能効果)を、商品パッケージに表示できる食品のことです。
機能性表示食品の制度は2015年から開始され、その届出総数は2023年5月末時点で7000件を突破しています。
機能性表示食品は特定保健用食品(トクホ)に比べると手続きが容易なうえ、対象となるヘルスクレーム(健康強調表示、機能性表示)が広いなど、事業者にとってさまざまなメリットもあることから参入が活発化。
消費者の健康志向の高まりも追い風となり、機能性表示食品の市場は順調に拡大を続けています。
2. 機能性表示食品の届出件数や人気の成分・機能性のランキング
次に、機能性表示食品の届出件数や人気の成分・機能性、体の部位のランキングをみてみましょう。
※データは2023年5月までのものから集計しています。
機能性表示食品の届出数推移
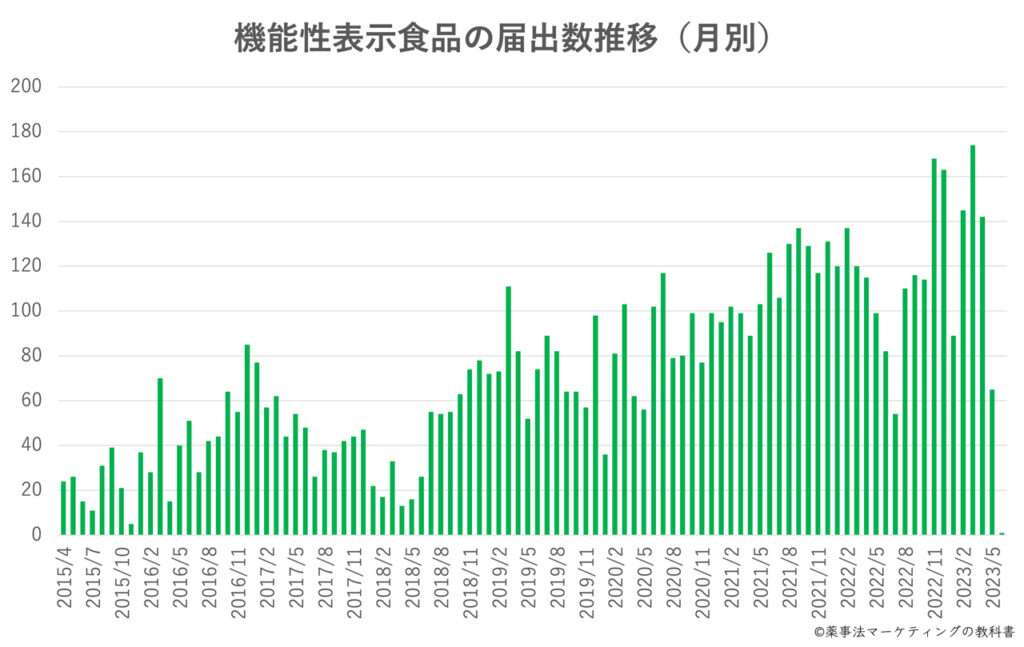
機能性表示食品の届出件数を月別にまとめたデータです。
一時的に届出件数が減少した月もありますが、機能性表示食品の制度の開始当初からみると、届出件数は増加傾向にあります。
機能性表示食品は2015年から制度が開始されましたが、その届出総数は2023年5月末時点で7000件を超えています。なお、届出の撤回総数は集計時点で合計706件となっています。
機能性表示食品の届出者ランキング
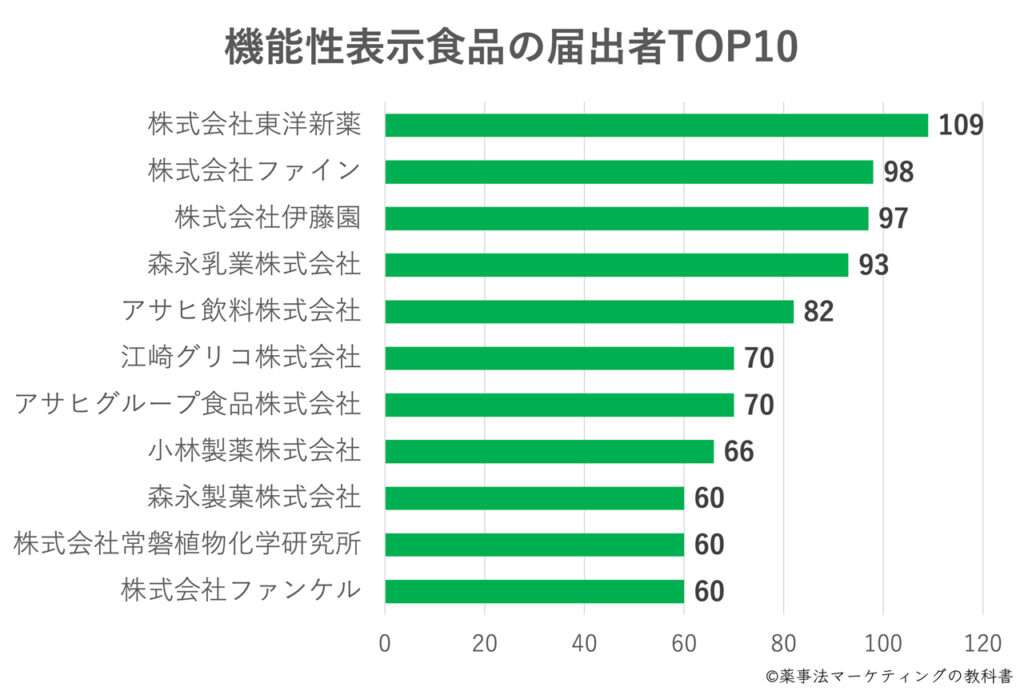
機能性表示食品の届出件数が多い企業のトップ10と届出件数をまとめたデータです。届出者数は合計1647でした。
届出者はさまざまで大手・中小問わず、食品メーカーや医薬品メーカーなどもみられました。
また、一般消費者を対象に商品を販売するBtoC企業だけでなく、企業から委託を受けて製造を請け負う「受託製造(OEM)」メーカーも多いのが特徴です。
機能性関与成分ランキング
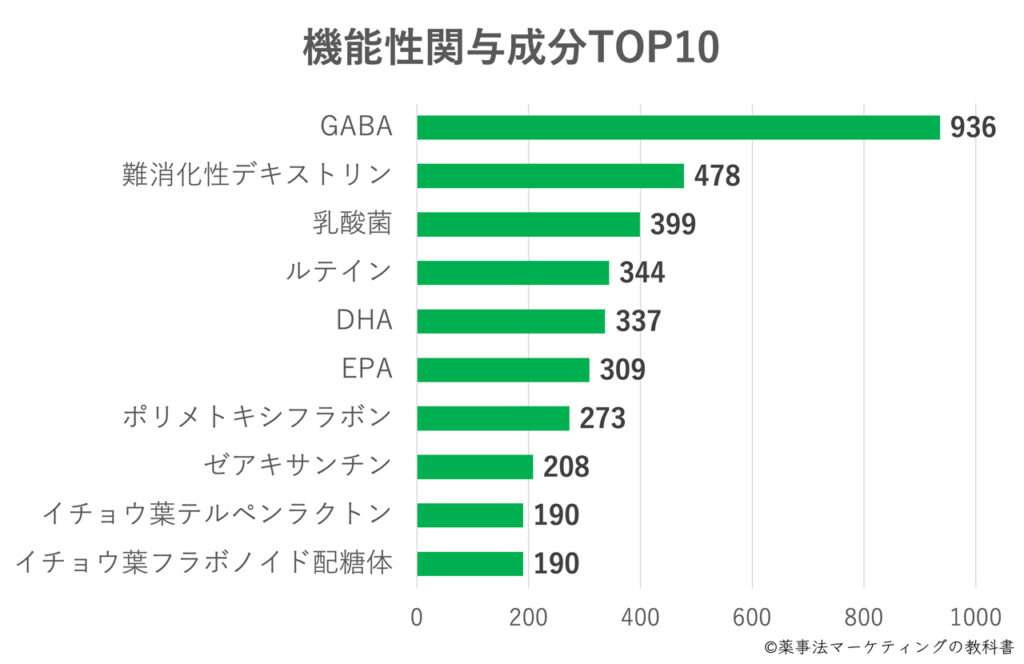
機能性関与成分の届出件数のトップ10をまとめたデータです。関与成分の種類は合計280でした(※当社の分類方法)。なお、一つの機能性表示食品で、複数の関与成分を含んでいるものもありますが、その場合は各成分を個別にカウントしています。
機能性関与成分で届出件数で多いのは「GABA」で900件以上にものぼります。GABAは「血圧」や「ストレス」を中心に、訴求できる機能性が幅広いことなどもあり、製品に利用されることが多く、近年、届出件数が増加しています。
表示しようとする機能性ランキング
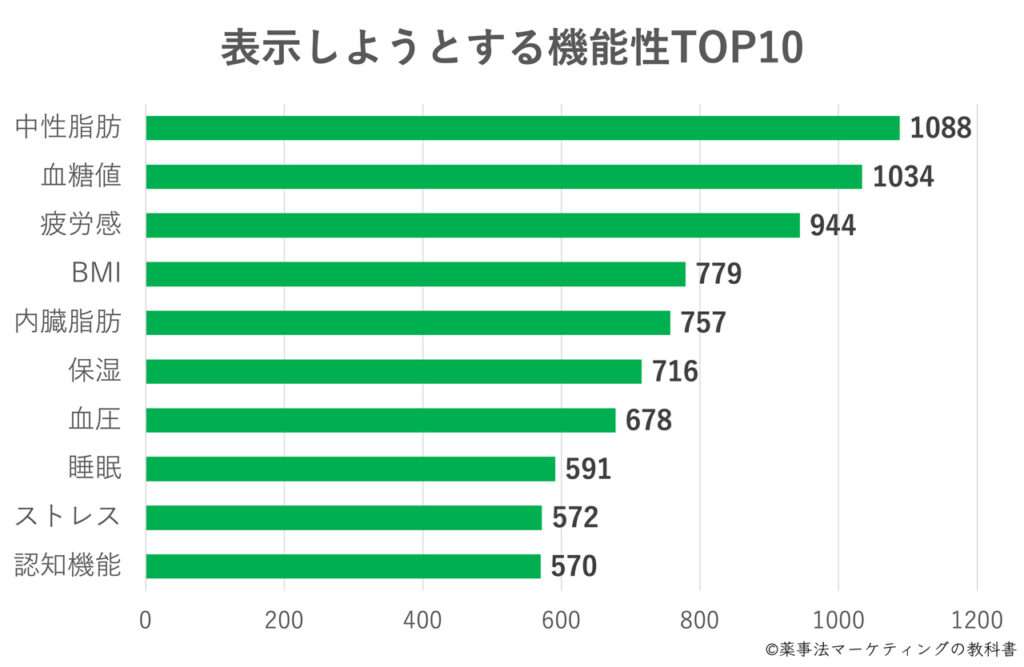
表示しようとする機能性のランキングです。表示しようとする機能性の種類は、少しずつ広がりをみせています。たとえば、新型コロナウイルスの感染拡大によって、「免疫」に関する機能性を表示した商品が増加するといった傾向もみられました。
今回は「中性脂肪」「血糖値」「疲労感」などがランキングの上位に入っており、そのほかに「睡眠」や「ストレス」も件数を伸ばしています。
体の部位ランキング
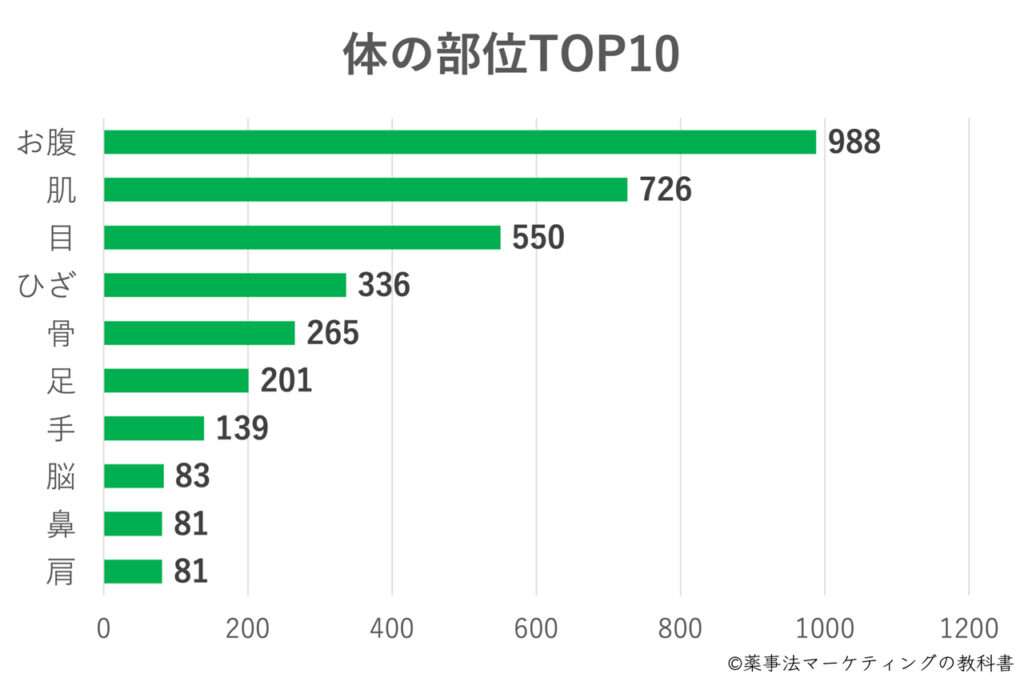
機能性表示食品では、企業の責任において科学的根拠(エビデンス)を示すことができれば、特定の「体の部位」を表示することも可能です。
機能性表示食品で多く表示された体の部位は、「お腹」「肌」「目」などです。
「お腹」が多い理由として、お腹の脂肪減少を狙ったダイエット系の商品だけでなく、腸内環境の改善を訴求した商品など、ニーズが幅広いことも一因と考えられます。
関与成分や表示しようとする機能性が多様化
機能性表示食品市場の活況に伴い、届出件数が増加し、機能性関与成分や表示しようとする機能性も広がりをみせています。
画期的なトピックとしては、「月経」を表示した初の機能性表示食品の登場が挙げられます。
アサヒグループ食品は「月経周期」に関する機能性表示食品として、2024年にサプリメント「わたしプロローグ」を発売すると発表しました。
「わたしプロローグ」は「CP2305ガセリ菌」を機能性関与成分とし、「女性の月経周期に関連した精神的疲労感や眠気の軽減」といった機能性を表示した商品。女性の健康課題をテクノロジーで解決する「フェムテック」領域の商品としても注目されています。
そのほか、「免疫機能」を表示した機能性表示食品も高い人気を集めています。
「免疫機能」の表示は、2020年にキリンビバレッジの「iMUSE(イミューズ)」で、機能性表示食品として初めて認められました。「iMUSE」は機能性関与成分として「プラズマ乳酸菌」を配合した、飲料やサプリメントなどのシリーズです。機能性として「健康な人の免疫機能の維持をサポート」を表示し、コロナ禍で消費者の健康や免疫への関心が高まるなか、ヒット商品となりました。
「iMUSE」の好調もあり、免疫領域にはその後、アサヒグループ食品やキユーピーも参入。アサヒグループ食品は「L‐92乳酸菌」、キユーピーは「酢酸菌GK-1」をそれぞれ機能性関与成分とした商品を発売し、売り上げを大きく伸ばすなど、機能性表示食品における免疫領域の市場が活性化しています。
近年の機能性表示食品の傾向をみても、免疫やストレス、睡眠など、消費者の健康ニーズは多様化が進んでいます。今後も新たな健康ニーズを開拓できる可能性は十分あるとみられ、機能性表示食品の市場は事業者にとって、まだまだ多くのビジネスチャンスが眠っているといえるでしょう。
3. 機能性表示食品の市場に関する今後の展望
機能性表示食品は商品の健康効果をアピールでき、売上増加が期待できることから、企業が続々と参入しています。
新型コロナウイルスの感染拡大の影響もあり、ストレスや睡眠の悩み、運動不足による肥満対策をはじめとして、消費者の健康意識は高まっています。
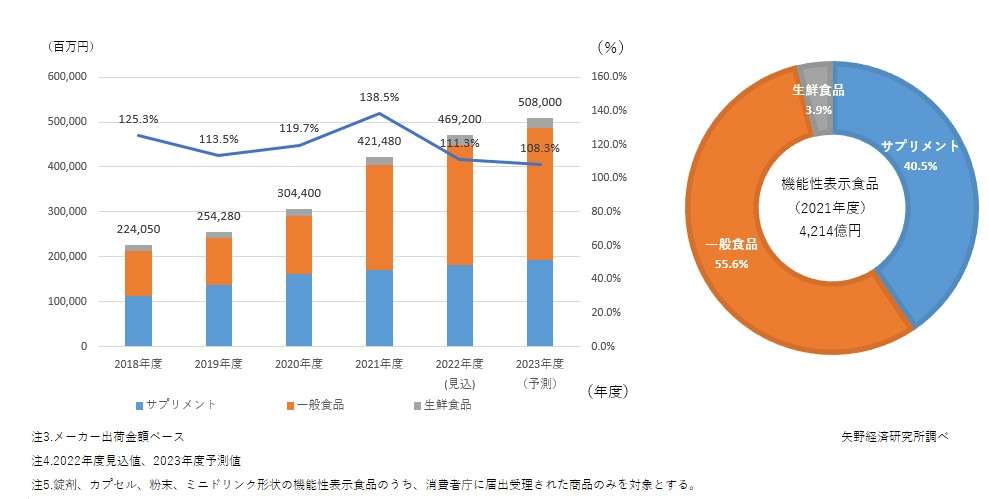
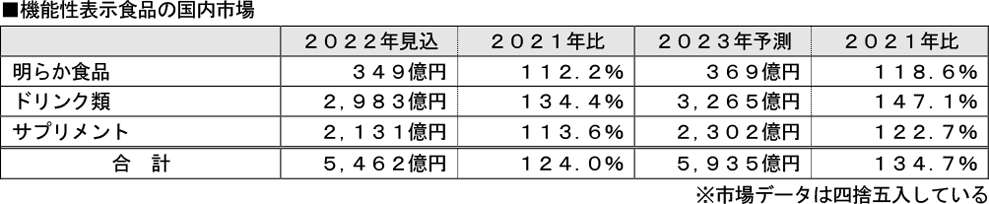
それに伴い、機能性表示食品の市場も堅調に推移。今後も、消費者の健康意識の高まりを背景に、機能性表示食品の市場は拡大するものと予想されます。
4. 【2023年の注目トピック】「科学的根拠」で初の措置命令
消費者の健康志向の高まりを背景に、健康食品市場が拡大するなか、薬機法や景品表示法に違反する企業も目立つようになりました。事態を重くみた国の取り締まりは、年々厳しくなってきています。
機能性表示食品で初となる「科学的根拠」での措置命令
2023年6月、さくらフォレストが販売する機能性表示食品のサプリメント「きなり匠」「きなり極」の広告に対し、消費者庁の表示対策課は景品表示法違反(優良誤認表示)として、措置命令を出しました。
「きなり」は機能性関与成分としてDHA・EPA(中性脂肪低下)などの成分や機能性を表示していました。
しかし、機能性表示食品の届出の際に提出した資料に関して、機能性を証明するのに科学的根拠(エビデンス)が不十分と判断され、処分を受けることになったのです。
科学的根拠を理由とした措置命令は、機能性表示食品として初であり、業界内でも大きなインパクトを与える事件となりました。
さくらフォレストが受けた措置命令の概要について、詳しく知りたい方はこちらをご覧ください。
▶︎ さくらフォレスト株式会社「令和5年6月30日」| 林田学監修:薬事法ドットコム措置命令データブック
措置命令を受けたさくらフォレストには、今後、課徴金納付命令が出されると予想されます。なお、景品表示法に違反した場合、課徴金額は対象商品の売上額の3%となります。
さくらフォレストの「きなり」は売上が大きな商品だったため、その3%となると課徴金は非常に多額になると見込まれます。
ところで、この「さくらフォレスト事件」は広告に違反があると判断されたわけですが、注目すべきなのは「広告表現」ではなく、「科学的根拠」が問題視されたことです。
企業は機能性表示食品の届出を国に出す際に、機能性の根拠となる論文などの資料も提出し、それらが受理されて商品の販売が可能となります。
そのため、すでに受理されている資料に対し、後からなぜ科学的根拠が不十分だと指摘するのか、と業界には衝撃が走りました。
機能性表示食品業界で勝ち抜くには「情報力」と「戦略力」が必要
2023年6月に起きた「さくらフォレスト事件」ですが、実はこの事件に関する調査は、消費者庁の表示対策課によって、すでに2022年後半から開始されていました。
なぜ私ども薬事法ドットコムが、こうした消費者庁の動きを把握していたのか。
薬事法ドットコムでは、薬機法に関するコンサルティングを行っており、数多くのクライアントがおります。
「さくらフォレスト事件」の調査と同時期に、私どものクライアントに対しても、別の機能性関与成分で調査が始まっていました。そのため、消費者庁の水面下の動きを把握できていたのです。
ただ、消費者庁の動きの背景まではわからなかったため、私どもはその背景を必死に探りました。
その背景について述べる前に、ここで機能性表示食品に関する消費者庁の権限分担について、簡単に説明しておきましょう。
機能性表示食品に関する消費者庁の権限分担は、非常に複雑です。
まず機能性表示食品の受理は「食品表示企画課」が担当します。届出完了後は「表示対策課」(景品表示法担当)などによる「事後チェック」があります。表示対策課は消費者庁が定める「事後チェック指針」に基づき、景品表示法などの観点から違反をチェックします。
つまり、機能性表示食品は届出が完了すれば終わりではありません。届出完了後も消費者庁でチェックが行われ、場合によっては企業が違反を問われることもあるのです。
機能性表示食品に関するこのような消費者庁の権限分担なども踏まえた、私どもの情報収集・分析の結果、消費者庁の2つの狙いが見えてきました。
1つめは、「事後チェック」を行い、取り締まりを厳しくすることで業界の健全化を図ること。機能性表示食品の市場が拡大するなか、広告表示の違反以外に、機能性の根拠とする資料の信頼性に対して、国から指摘を受ける事例も目立ち始めていたことも要因の一つと考えられます。
2つめは、事後チェックとそれに伴う企業への措置命令を、消費者庁の人事異動が行われる2023年7月1日より前に実現すること。
私どもはこうした狙いがあるとみて、消費者庁の調査に関して対応を実施。その結果、私どものクライアントに関しては、国から問題視される事態を防ぐことができました。
それに対して、さくらフォレストは国の調査や動向に関する情報力や戦略力もなく、消費者庁の表示対策課が描いたシナリオどおりに措置命令に至った、といえます。
機能性表示食品の業界は、薬機法などの法律や「機能性表示食品の届出等に関するガイドライン」などを理解することが基本です。
機能性表示食品に関するガイドラインに関して、詳しく知りたい方はこちらをご覧ください。
しかし、法律やガイドラインを理解しただけでは十分ではありません。国から指摘を受けた場合など不測の事態に対応するためには、法律関連の知識だけでなく、国の動向なども含めた高度な「情報力」と「戦略力」も必要となります。
選ばれる理由は高度な情報力と戦略力!薬事法ドットコムの機能性表示食品のコンサルティングについて、詳しく知りたい方はこちらをご覧ください。
5. 機能性表示食品の最新トレンドと今後必要な対策とは?
機能性表示食品の市場は順調に拡大を続けていますが、その反面、競争が厳しいのが実情です。
その厳しい競争のなかで勝ち残っていくために、押さえておきたい機能性表示食品の最新トレンドと、今後必要な対策について解説します。
競争激化によって「マルチヘルスクレーム」などの差別化が求められる
機能性表示食品は、消費者の健康志向の高まりに加え、事業者からすると特定保健用食品(トクホ)に比べると手続きが容易なうえ、対象となるヘルスクレーム(健康強調表示、機能性表示)が広いなどもメリットもあり、市場が拡大しています。
今後、増加が予想される機能性としては、現代社会の悩みを反映した「ストレス」や「睡眠」のほか、高齢化社会の進行に伴い、関心が高まっている「認知機能」が挙げられます。それ以外だと、女性の健康課題を解決する「フェムテック」関連の機能性も、今後の需要増加が見込まれます。
また、機能性表示食品の市場における競争が激化するなか、勝ち残っていくためにはさらなる差別化が必要となります。
差別化戦略の一つとして挙げられるのが、複数のヘルスクレームを組み合わせた「マルチヘルスクレーム」です。マルチヘルスクレームは複数の機能性を表示でき、高い訴求力が期待できることから、今後ますます広がることが予想されます。
届出に関する新ガイドラインへの対応
機能性表示食品は制度面でも大きな見直しが行われ、事業者はこうした変化にも対応していく必要があります。
具体的な例を挙げると、消費者庁は2023年9月、「機能性表示食品の届出等に関するガイドライン」の一部改正を行いました。
改正点のなかでも特に重要なのは、届出資料として用いられる研究レビュー(SR)の科学的根拠に対して、より確実性や信頼性が求められるようになったことです。
これまでは、簡単にいえば、表示しようとする機能性に関する論文が7つあったとして、そのうち5つが肯定的な論文であればOKでした。
今回の改正によって、表示しようとする機能性に関する肯定的な論文の数が、否定的な論文の数よりも少ない場合は、肯定的な論文の「前提」(その根拠を示すにあたって前提となる条件)も問われるようになりました。
たとえば、届出を出した製品と肯定的な論文とで、用いられている成分の含有量が同じかどうか、といったことも重要となります。
そのほかの主な改正点としては、以下の点が挙げられます。特に機能性表示食品の届出を行う事業者の方は、理解しておきましょう。
「PRISMA声明(2020年)」への準拠
「PRISMA声明」とは、研究レビュー(SR)の報告に関する国際指針のこと。
これまでガイドラインが準拠していたPRISMA声明が「2009年版」から「2020年版」に更新されたことに伴いで、PRISMA声明チェックリストなどが一部変更となりました。
届出内容の責任の所在を明確にすること
届け出た内容(たとえば、科学的根拠など)に対する責任の所在を明確にするため、届出資料作成におけるチェックリストに、届出者(個人または法人)の代表者の確認欄が追加されました。
30日ルールの廃止
改正前は、事業者団体等の事前チェックを受けた届出資料に関して、消費者庁は30日以内に届出を受理(もしくは差し戻し)を判断するという運用が行われていました(30日ルール)。これには、消費者庁の確認作業を迅速化し、チェック期間を短縮するなどの目的がありました。ただ、今回の改正によって、30日ルールはガイドラインから削除されています。
臨床試験機関の選び方も重要に
競争が激しい機能性表示食品の市場で勝ち抜くためには、生産コストを抑えることも一つの手です。
たとえば、すでに多くの受理件数がある機能性関与成分でも、効果はそのまま維持しつつ、製品に含まれる成分量を少なくできれば、生産コストを大幅に削減でき、企業の競争力向上につながります。
これを実現するには、製品の機能性の科学的根拠を証明するための臨床試験(RCT)を行う、臨床試験機関との連携が欠かせません。ただ、どの検査機関でも実現できるわけではなく、高い技術力と豊富な実績を持つ検査機関を選ぶことが重要です。
おすすめなのは、薬事法ドットコムのグループである日本臨床試験協会(JACTA)です。
一般的な検査機関は「臨床試験は研究のために行う」というスタンスであり、必ずしも製品の広告の訴求ポイントを裏づける結果を出してくれるとは限りません。
その点、JACTAは薬事法ドットコムと連携して、企業が広告で訴求したいポイントなども踏まえた臨床試験を実施します。
たとえば、「イヌリン」という成分の場合、効能効果を得るには、他社製品だと摂取量が8g以上必要でした。それに対し、JACTAでは臨床試験を通じて、わずか1gの摂取で効果があるという結果を導き、業界に大きなインパクトを与えました。
このような科学的根拠に基づいた試験結果が得られれば、効果は維持しながら、成分の含有量を減らして生産コストを削減する、といったことが可能となり、企業にとって大きなメリットといえるでしょう。
日本臨床試験協会(JACTA)について、詳しく知りたい方はこちらをご覧ください。
6. 機能性表示食品の届出・広告はプロにサポートを依頼
機能性表示食品は市場拡大が続く一方、競争も激化。厳しい競争を勝ち残るための対策として、「マルチヘルスクレーム」などの差別化や、新たなガイドラインへの対応などがあります。
しかし、「さくらフォレスト事件」からわかるように、一度国に受理された資料が科学的根拠で違反を問われるなど、薬機法やガイドラインなどの知識だけでは対応しきれない問題が発生する可能性があります。
こうしたリスクを防ぐためには、国や行政の水面下での動向なども含めてキャッチする高い「情報力」と、それに対する「戦略力」が重要になります。
したがって、機能性表示食品の届出や広告は事業者だけで行うのではなく、機能性表示食品の専門家にサポートを依頼するのが安心といえるでしょう。
7. 機能性表示食品のコンサルティングなら薬事法ドットコムへ
機能性表示食品のコンサルティングなら、薬事法ドットコムがおすすめです。薬機法など関連する法律の知識はもちろん、国や行政などの水面下の動きもキャッチする高い「情報力」と、それに対する「戦略力」が強みです。
最新情報がわかる!無料のメールマガジン配信中
薬事法ドットコムでは、機能性表示食品の最新情報が読める、無料のメールマガジンを配信していま
す。機能性表示食品に関する法改正や注意点のほか、薬事法ドットコムならではの情報網を活かした業界の水面下の情報まで、最新情報をどこよりも早く提供いたします。
機能性表示食品の届出受理には、科学的根拠の確実性はもちろんですが、それだけでなく、制度の運用に関する国や業界の戦略・思惑が絡んでいることもあります。
薬事法ドットコムでは卓越したリサーチ力を活かし、こうした背景も含めて届出の受理基準を分析。その結果、機能性表示食品として初めて「免疫機能」の表示が認められた、キリンビバレッジの「iMUSE(イミューズ)」のヘルスクレームの受理基準について予想を的中させました。
そのほか、「さくらフォレスト事件」の情報や見解もいち早く配信し、業界内で大きな反響を呼びました。
薬事法ドットコムでは機能性表示食品に関する最新情報を配信中! 無料のメールマガジンはこちらからご登録ください。
機能性表示食品の届出からエビデンス作成まで一貫してサポート
薬事法ドットコムでは、機能性表示食品の届出や広告表示、臨床試験(RCT)をはじめ、薬機法に関するさまざまなコンサルティングを行っています。
機能性表示食品の届出サポートについても、豊富な実績があります。
薬事法ドットコムの機能性表示届出(2026年4月1日現在)
関与実績
187件
受理実績
78件
日本初プロデュース
14件
- 関与実績 187件
- 受理実績 78件
- 日本初プロデュース 14件
薬事法ドットコムなら研究レビュー(SR)や臨床試験(RCT)に基づく「エビデンス作成」から「届出書類の作成」まで一貫して対応。また、関連組織には「日本臨床試験協会(JACTA)」もあり、臨床試験を含めたサポートも可能です。
薬事法ドットコムによる機能性表示食品のコンサルティングの料金について、詳しく知りたい方はこちらをご覧ください。
薬事法ドットコムでは無料相談にも対応しております。機能性表示食品のことでお困りでしたら、ぜひお気軽にご相談ください。


