2023年10月19日更新
機能性表示食品の広告は「景品表示法」や「健康増進法」などの法律に加え、「適正広告自主基準」や「事後チェック指針」といった、広告に関するガイドラインも遵守しなければなりません。
もし違反すれば、措置命令や課徴金納付命令などのペナルティーを受ける可能性があり、注意が必要です。
そこで本記事では、機能性表示食品の広告に関する法律やガイドライン、注意点から、広告表現のNG例までわかりやすく解説。
この記事を読めば、機能性表示食品の広告で押さえておくべきポイントがしっかりつかめます。
機能性表示食品とは?広告に該当するものは?
はじめに、機能性表示食品の概要と、その広告に該当するものとは何か、基本的なところから知っておきましょう。
機能性表示食品とは
機能性表示食品とは「おなかの調子を整えます」「脂肪の吸収をおだやかにします」など、健康の維持・増進に役立つ食品の機能性(効能効果)を、商品パッケージに表示できる食品のことです。
事業者が食品の安全性や機能性に関する科学的根拠(エビデンス)などの情報を、消費者庁に届け出れば、国の審査なしに、事業者自らの責任で機能性の表示ができます。
「機能性表示食品」制度は、2015年4月に開始。
この制度により、消費者にとっては、機能性がわかりやすく表示された商品の選択肢が増え、自身の目的に合った商品を選択しやすくなりました。
一方、事業者にとっては、商品の健康効果をアピールできるため、マーケティング面でメリットがあり、売上増加が期待できます。
また、機能性表示食品は、特定保健用食品(トクホ)と比べて、手続きが容易なうえ、対象となるヘルスクレーム(健康強調表示、機能性表示)の範囲が広いのも特徴です。
こうした背景もあり、機能性表示食品制度の利用は順調に拡大。機能性表示食品が登場する24年前に始まった、トクホを上回る件数がすでに受理され、市場に広く流通しています。
▼機能性表示食品について詳しく知りたい方は、こちらの記事もご覧ください。
▶「機能性表示食品とは?」を丸ごと解説
機能性表示食品の広告に該当するもの
機能性表示食品の広告を行ううえで、まず「どのようなものが広告に該当するのか」を知っておく必要があります。
機能性表示食品を含む、食品の虚偽・誇大広告の禁止などについて定めている健康増進法では、以下の3つの要件すべてに該当する場合、広告に該当するとしています。
- 顧客を誘引する(顧客の購入意欲を昂進させる)意図が明確にあること。
- 特定食品の商品名等が明らかにされていること。
- 一般人が認知できる状態であること。
また、広告の具体例としては以下のものがあります。
- 商品(サンプルを含む。)、容器又は包装による広告その他の表示及びこれらに添付した物による広告その他の表示
- 見本、チラシ、パンフレット、説明書面その他これらに類似する物による広告その他の表示(ダイレクトメール、ファクシミリ等によるものを含む。)及び口頭による広告その他の表示(電話によるものを含む。)
- ポスター、看板(プラカード及び建物又は電車、自動車等に記載されたものを含む。)、ネオンサイン、アドバルーンその他これらに類似する物による広告等及び陳列物又は実演による広告
- 新聞紙、雑誌その他の出版物、放送(有線電気通信設備又は拡声機による放送を含む。)、映写、演劇又は電光による広告
- 情報処理の用に供する機器による広告その他の表示(インターネット、パソコン通信等によるものを含む。)
このように、広告に該当する範囲は非常に広いことがわかります。機能性表示食品の製造・販売を行う事業者は、広告の表示内容が法律に抵触していないか、広範囲にわたって注意する必要があります。
機能性表示食品の広告の注意点・ポイント
では機能性表示食品の広告では、どのような点に注意する必要があるのでしょうか。具体的なポイントをお伝えします。
機能性表示食品の広告における必要・禁止事項
①表示内容の科学的根拠
機能性表示食品の表示内容は、科学的根拠(エビデンス)に基づくものでなければいけません。
機能性表示食品では事業者の責任で、機能性や安全性に関する試験や調査を行う必要があります。
その方法として、「臨床試験」と「研究レビュー」の2つがあります。
臨床試験(RCT:Randomized Clinical Trial)
人を対象とし、最終商品(商品の完成品)を用いて、成分・食品の摂取が健康状態などに及ぼす影響を評価する。
研究レビュー(SR:Systematic Review)
▼エビデンスの作成について詳しく知りたい方は、こちらの記事もご覧ください。
▶ エビデンスの作成
②表示範囲の明確化
機能性表示食品は、目的や対象者などの範囲を明確に表示しなければなりません。
機能性表示食品は、疾病の診断・治療・予防を目的とした「医薬品」ではなく、「食品」に分類される「保健機能食品」のうちの一つです。
そのため、「疾病の診断・治療・予防を目的としたものではない(医薬品ではない)」ことを明記する必要があります。
また、対象者についても「疾病のある方や未成年者、妊産婦(妊娠を計画している方を含む)、授乳中の方を対象に開発された商品ではない」といった表示も必要になります。
③医薬品的な表現の禁止
機能性表示食品はいくら科学的根拠(エビデンス)があっても、医薬品ではないため、疾病の治療・予防効果を暗示する表示はできません。
また、「肉体改造」「増毛」「美白」など健康の維持・増進の範囲を超えた表現も使用できません。
このような医薬品と誤解を招く表現は、薬機法の規制対象となります。
※ただし、健康維持・増進の範囲内であれば、身体の特定の部位(肌やおなかなど)に言及した表現も可能です。
機能性表示食品であっても、「認められる表現」と「認められない表現」があるので注意しましょう。
| 容易に測定可能な体調の指標の維持に適する または改善に役立つな どの表現 | 「血圧が高めの方に」 「体に脂肪がつきにくい」 「中性脂肪を低下させる」 など |
|
身体の生理機能、組織機能の良好な維持に適する または改善に役立つなどの表現 | 「目のピント調節機能改善」 「目の疲労感の緩和」 「糖の吸収を抑えます」 など |
|
身体状態を本人が自覚でき、 一時的な体調の変化(継続的、慢性的でないもの) の改善に役立つなどの表現 | 「一時的なストレスの低減」 「一時的な疲労感の緩和」 「VDT作業時の一時的な目の不快感」 など |
|
| 病気の予防・診断・治療効果を暗示する表現 | 「糖尿病の疑いがあるあなたへ」 「花粉症が治ります」 「風邪の予防に」 など |
|
健康の維持・増進の範囲を超えた、 意図的な健康の増強を主張する表現 |
「ガイドライン」を遵守する
機能性表示食品の広告に関するルールは「機能性表示食品の届出等に関するガイドライン」(消費者庁)で定められています。
たとえば、以下にあるように、商品パッケージに記載すべき事項などが具体的に示されています。
<パッケージ表>
- 機能性表示食品である旨
- 届出番号
- 消費者庁長官に届け出た機能性
<パッケージ裏>
- 1日当たりの摂取目安量
- 摂取方法
- 注意事項
- 医薬品ではない旨
- 疾病の罹患者、未成年者、妊産婦(妊娠を計画している方を含む)および授乳婦を対象に開発された食品ではない旨
- 「食生活は、主食、主菜、副菜を基本に、 食事のバランスを。」という食事のバランスに関する記述
- 事業者の連絡先
- 1日当たりの摂取目安量当たりの機能性関与成分の含有量
ガイドラインを逸脱した広告は、法律違反となるおそれがあります。機能性表示食品の広告を行う際は、必ずガイドラインを遵守するようにしてください。
機能性表示食品の広告に関しては、国や行政からガイドラインなどさまざまな情報が公表されています。しかし、専門的な知識がないと理解が難しいのも事実です。
もし、機能性表示食品の広告や表示で法律違反となると、業務停止命令や罰金などのペナルティーを受ける可能性があり、経営面で大きな損害を受けるおそれも。
こうした事態を防ぐために、機能性表示食品の届出や広告のことなら、専門家に相談するのが安心です。
薬事法ドットコムでは無料相談を実施していますので、お気軽にご相談ください。
機能性表示食品の広告に関連する法律
機能性表示食品の広告に関連する主な法律として、「景品表示法」「健康増進法」「食品表示法」があります。
たとえば、科学的根拠情報の範囲を超えた広告表示は「景品表示法の不当表示」や「健康増進法の虚偽誇大広告」に該当するおそれがあります。
また、国に届け出た「機能性関与成分」以外の成分を強調した表現などは、「食品表示法」違反となる可能性があります。
以下に、「景品表示法」「健康増進法」「食品表示法」のなかでも、機能性表示食品の広告と関連性の高いルールをまとめていますので、確認しておきましょう。
景品表示法
優良誤認表示の禁止(4条1項1号)
商品の品質、規格その他の内容について、実際のものや競争事業者のよりも著しく優良であると一般消費者に示す表示を禁止
不実証広告規制(4条2項)
優良誤認に該当する表示か否かを判断するため必要があると認めるときは、事業者に対し、期間を定めて、当該表示の裏付けとなる合理的な根拠を示す資料の提出を求めることができる
健康増進法
誇大表示の禁止(31条1項)
何人も、食品の健康保持増進効果等について、著しく事実と相違する表示又は著しく人を誤認させる表示を禁止
食品表示法
食品表示基準(表示禁止事項のうち主なもの)
- 実際のものより著しく優良又は有利であると誤認させる用語
- 機能性表示食品にあっては、次に掲げる用語
- 疾病の治療効果又は予防効果を標榜する用語
- 消費者庁長官に届け出た機能性関与成分以外の成分を強調する用語
- 消費者庁長官の評価、許可等を受けたものと誤認させるような用語
- 栄養成分の機能を示す用語
- 保健機能食品以外の食品にあっては、保健機 能食品と紛らわしい名称、栄養成分の機能及び特定の保健の目的が期待できる旨を示す用語
- その他内容物を誤認させるような文字、絵、写真その他の表示
機能性表示食品広告のNGとポイント
機能性表示食品の広告では、具体的にどのような表示や表現が可能なのでしょうか。
ここでは、機能性表示食品の広告表現のNG例のほか、広告にグラフを用いる場合のポイントもお伝えします。
広告表現のNG例
届出表示の省略・簡略化
【届出表示】
本品には○○(機能性関与成分の名称)が含まれます。○○には、血中コレステロールを低下させる機能があることが報告されています。
【NG例】
コレステロールを下げる
【NG理由】
商品自体に「コレステロールを下げる」機能があると、消費者の誤認を招く可能性があるため。
届け出た「機能性関与成分」以外の成分の機能を強調
【届出表示】
機能性関与成分が「難消化性デキスト リン」
【NG例】
難消化性デキストリンおよび大豆イソフラボンが含まれるので、内臓脂肪を減らすのを助ける機能があります。
【NG理由】
「大豆イソフラボンも機能性関与成分である」という印象を消費者が抱く可能性があるため。
広告にグラフを用いる場合のポイント
次に、広告にグラフを用いる場合に、押さえておきたいポイントをお伝えします。
例)
食後の血糖値上昇を抑える機能性表示食品の広告で、血糖値のグラフを掲載する場合
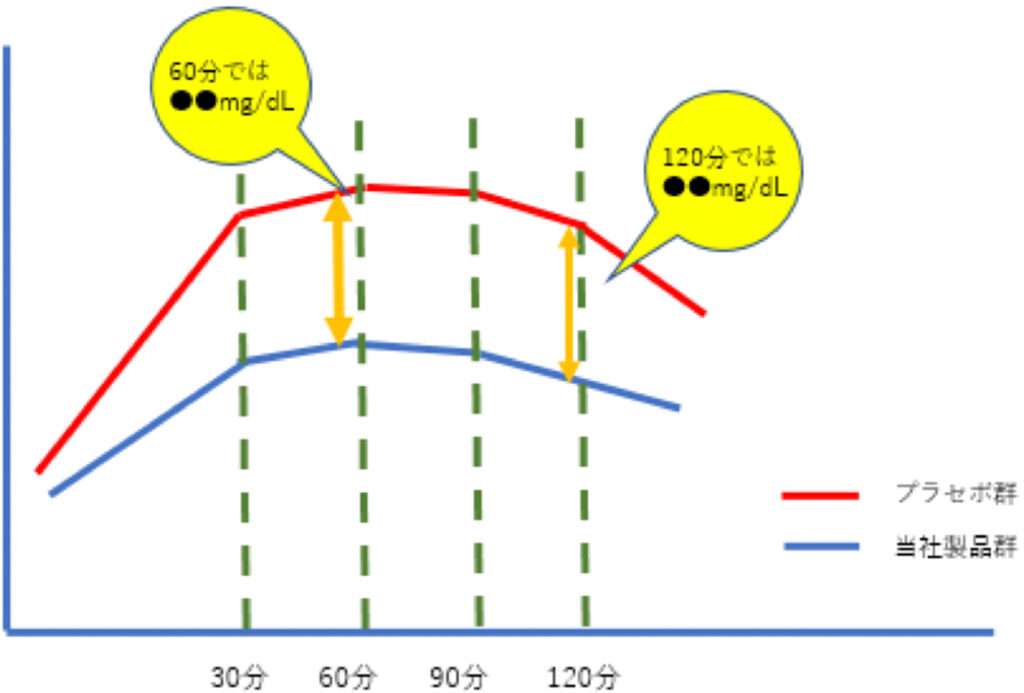
消費者庁の「機能性表示食品の事後チェック指針」によると、広告にグラフを用いることは認められています。
ただ、グラフを使用する際は、消費者の誤解を招かないよう、場合によってはグラフに補足説明を加える必要があります。
たとえば、今回、例に挙げたグラフが臨床試験ではなく、研究レビューに基づく情報である場合、その旨を明記しなければなりません。
参考:機能性表示食品に対する食品表示等関係法令に基づく事後的規制(事後チェック)の透明性の確保等に関する指針(消費者庁)
グラフに追加すべき補足説明・ポイント
- グラフが本品を用いた結果ではなく、研究レビューで採用した文献の結果であること
- その文献を選択した理由(機能性関与成分の含有量が本品と同等で、代表的な論文であること等)
-
グラフの結果を導いた試験の条件
例)被験者が食後血糖値高めの方(境界域の方)であるならば、その旨を明記する - 特定のポイントだけ取り上げて強調しないように注意する
機能性表示食品の広告が、法律に違反していないかという判断は、専門知識がないと難しいものです。機能性表示食品の広告のことなら、薬事法ドットコムへお気軽にご相談ください。
機能性表示食品の広告に関する違反事例
実際に、機能性表示食品の広告に関して、どのような違反事例があったのか、主なものをご紹介します。
「葛の花由来イソフラボン」で16社に措置命令(2017年11月)
2017年11月、消費者庁は「葛の花由来イソフラボン」を含む機能性表示食品を販売する16社に対し、景品表示法に基づく措置命令を出しました。
当該商品を摂取しただけで、誰でも簡単に痩せられるかのような広告表示が、景品表示法の「優良誤認表示」にあたると判断したためです。
措置命令が出された各事業者は、再発防止策の実施や新聞などへの謝罪広告の掲載が命じられました。
本件の場合、問題となったのは広告表示であり、機能性表示の届出の撤回を求められたわけではありませんでした。そのため、措置命令後も販売を継続している商品もあります。
「認知機能」広告を一斉監視、115社に行政指導(2022年3月)
2022年3月、消費者庁は「認知機能」の改善をうたう機能性表示食品を販売する115社に対して、景品表示法や健康増進法に違反するおそれがあるとして、行政指導を行いました。
問題となったのは、物忘れや認知症の治療・予防など医薬品的な効果効能が得られるかのような広告表示。
こうした広告表示が消費者の誤認を招くとして、景品表示法の「優良誤認表示」や健康増進法の「食品の虚偽・誇大表示」に抵触する可能性があると判断されたのです。
その結果、行政指導の対象となった事業者は、広告表示の改善が求められました。
ただ、本件の場合も問題となったのは広告表示であるため、機能性表示の届出の撤回は求められていません。
昨今、届出表示の範囲を逸脱したインターネット広告が広がっている状況もあり、消費者庁は機能性表示食品の届出後の「事後チェック」体制の強化が求められています。
本件はその一環として、消費者庁がインターネットにおける健康食品などの虚偽・誇大広告の一斉監視を行ったことが発端でした。
本件を通じて、事業者側も法規制に対応し、 適切な広告表示とそのチェックを行う必要性が浮き彫りとなった事例といえるでしょう。
「歩行能力の改善」で薬機法違反、届出撤回を要請(2018年11月)
2018年11月、消費者庁は「歩行能力の改善」 をうたう機能性表示食品を販売する12社に対して、届出表示の撤回を要請しました。
問題となったのは、食品にもかかわらず、「歩行機能の改善」という医薬品的な効果効能を表示した点です。
これを厚生労働省が薬機法に抵触するおそれがあると問題視。 厚生労働省の指摘を受け、消費者庁は当該事業者に対し、届出表示の撤回を求めました。
結果として、事業者は機能性表示食品の届出表示の変更が必要となり、各社が届出を撤回・出し直すことになりました。
不適切な成分名で、小林香料が「HMB」の届出撤回(2020年1月)
広告表示や届出表示だけでなく、機能性関与成分の成分名が問題となる場合もあります。
2020年1月、小林香料(株)が販売するサプリメントに配合されている「HMB」という機能性関与成分名が適切ではないとして、届出を撤回・出し直し、「HMBカルシウム」へ成分名が変更になったという事例です。
当該商品に配合されているのが「HMBカルシウム」であるにもかかわらず、「HMB」を機能性関与成分として、国に届け出ていたためです。
食品表示法の食品表示基準では、機能性表示食品は「消費者庁に届け出た成分を表示する」ことが義務付けられています。
そのため、商品で表示している機能性関与成分名が不適切であれば、届出を撤回・出し直す必要があります。
なお、本件の場合、厳密には広告表示というより、成分名に関する問題です。
広い意味では科学的根拠(エビデンス)の問題といえるかもしれませんが、成分名が不適切だっただけで、科学的根拠そのものの有効性を問われたわけではありません。
不十分な科学的根拠でさくらフォレストに措置命令(2023年6月)
さくらフォレストが販売する機能性表示食品のサプリメント「きなり匠」と「きなり極」について、消費者庁は2023年6月、景品表示法(優良誤認表示)に違反するとして措置命令を出しました。
「きなり」はDHA・EPA(中性脂肪低下)、モノグルコシルヘスペリジン(血圧低下)、オリーブ由来ヒドロキシチロソール(LDLコレステロールの酸化抑制)といった成分や機能性を表示。
しかし、同社が機能性の根拠として提出した論文が示す数値に対して、「きなり」に含まれるDHA・EPAの量が少ないなどの点から、資料は科学的根拠(エビデンス)として不十分と判断され、処分に至りました。
厳密にいえば、本件の措置命令は広告表示ではなく、科学的根拠の違反を理由としたものでした。
しかしながら、同社の積極的な広告展開などがきっかけとなり、消費者庁から商品の科学的根拠が疑問視され、調査・処分の対象となったようです。
本件は機能性表示食品の広告を取り扱ううえで、届出表示だけでなく、機能性の根拠とするデータが適切かどうかも重要だと改めて示す事例といえるでしょう。
機能性表示食品の広告に関する今後の展望
今後の機能性表示食品の広告に関する規制の見通しや、市場動向についても知っておきましょう。
機能性表示食品の広告規制の見通し
機能性表示食品は、機能性に関する科学的根拠(エビデンス)を消費者庁に届け出れば、国の審査なしに機能性の表示ができます。そのため、科学的根拠として不十分な研究レビュー(SR)でも届出が受理されることも多いのが現状です。
しかし、2023年の「さくらフォレスト事件」以降、仮に機能性の根拠として不十分な資料で届出が認められても、後に消費者庁から「事後チェック指針」を根拠に措置命令、さらには課徴金納付命令を受けかねない、というリスクが明らかになりました。
この事例から、今後、機能性表示食品の広告規制は、より強化されていくことも予想されます。
さくらフォレストの場合、同社が販売するサプリメント「きなり匠」「きなり極」に含まれるDHA・EPAの有効性を示す論文を根拠資料として提出しました。
しかし、提出された論文の大半が「きなり」の配合量の倍近い量で検証したものであるなど、矛盾点が厳しく指摘され、結果として措置命令を受けることになりました。
このことからも、今後、機能性表示食品の届出では、成分の摂取量とその結果を示す文献について、より慎重に取捨選択する必要があるといえます。
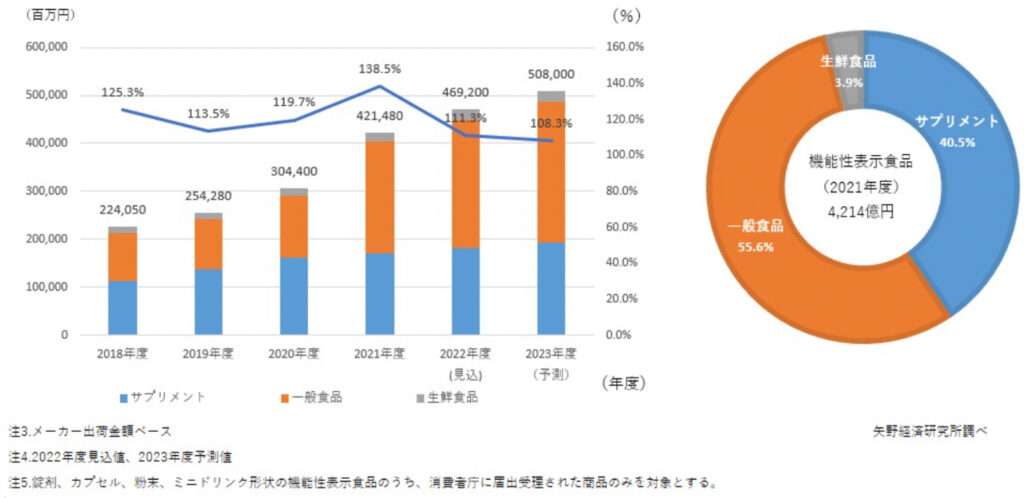
機能性表示食品の今後の市場動向
前述したように、機能性表示食品は商品の健康効果をアピールでき、売上増加が期待できることから、企業が続々と参入しています。
また、新型コロナウイルス感染症拡大の影響もあり、ストレスや睡眠問題、運動不足による肥満への対策など、消費者の健康意識は高まっています。
それに伴い、機能性表示食品の市場も堅調に推移。今後も、消費者の健康意識の高まりを背景に、機能性表示食品の市場は拡大するものと予想されます。
機能性表示食品の市場規模推移と食品種類別構成比(2021年度)