再生医療でお悩みではないですか?
再生医療の厚生労働省への届け出についてご相談下さい。
2014年11月25日より再生医療等の安全性の確保等に関する法律が施行され、再生医療を行う医療機関は「再生医療等委員会」の承認を経て厚生労働省に届出を行わないと、再生医療が実施できなくなりました。ところが、この新制度に対する認識が甘い医療機関もあり、届出を行うことなく従前の再生医療を続けて業務停止命令を受ける医療機関も出ている他、さい帯血事件では医師の逮捕にまで至っています。
手続きさえしっかり守っていればこういう事態に至ることはないのですが、手続きが分かりにくくこのような事態に至っています。
そのようなリスクを排除すべく、YDCがみなさまのナビゲート役を務めます。

どのような医療が対象となりますか
YDCは、第二種、第三種の治療または研究の審査のサポートが可能です。
たとえば次のようなメニューです。
- PRPによる肌再生・毛髪再生(第三種)
- PRPによるインプラント治療(第三種)
- Tリンパ球・NK細胞による免疫療法(第三種)
- PRPによる関節症治療(第二種)
- 線維芽細胞による肌再生(第二種)
- 脂肪由来幹細胞による関節症治療(第二種)
- 脂肪由来幹細胞による不妊治療(第二種)
- 脂肪由来幹細胞による糖尿病治療(第二種)
第一種・第二種・第三種再生医療等技術のリスク分類
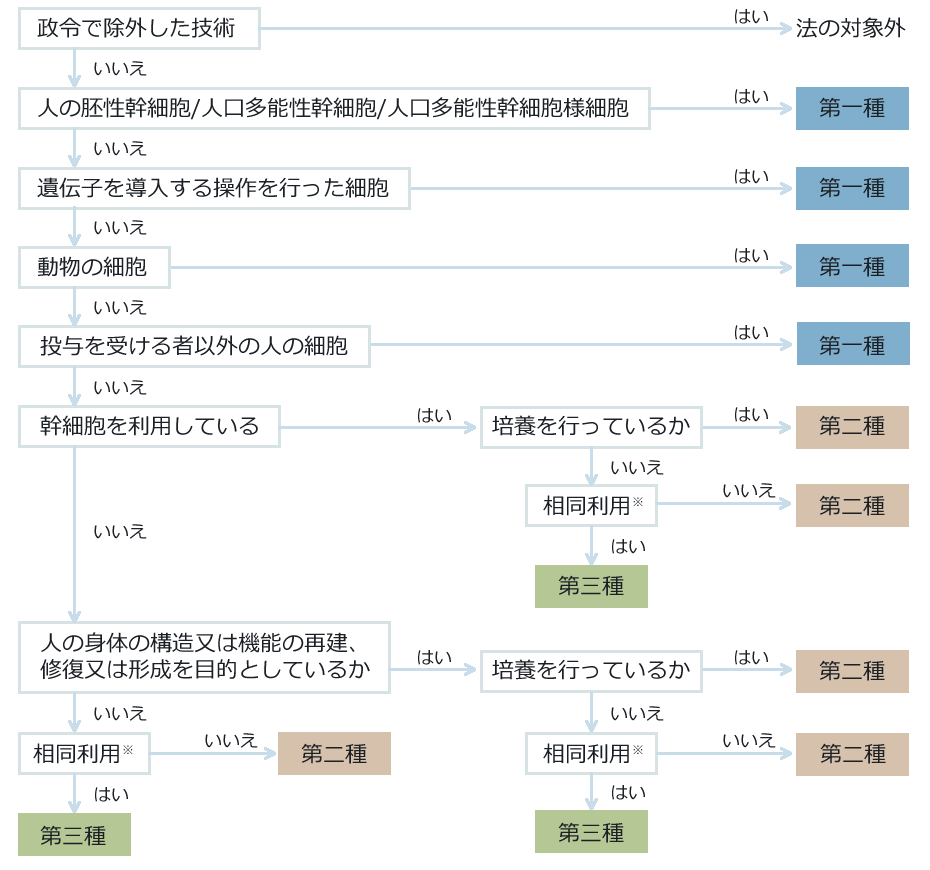
※関節腔内等、血流の乏しい組織への投与は相同利用に該当しない。
「医政研発 1031 第 1 号」より
どのような届出が必要になりますか
1. 新しく再生医療を始める場合 ⇒ 新規計画*
2. 既に再生医療の届出をしていたが、
(1) 場所を移転した場合 ⇒ 計画変更**
(2) クリニックから医療法人に組織変更した場合 ⇒ 新規計画***
3. 再生医療を行う医師が変わった(増えた)場合 ⇒ 計画変更
*院内で特定細胞加工物を製造される場合は、事前の「特定細胞加工物製造届」が必要です。
** 院内に細胞培養加工施設がある場合は、従前の特定細胞加工物製造の届出を廃止し、新規に特定細胞加工物製造の届出が必要です。
*** 従前の再生医療等提供計画について中止の届出が必要です。
届出が必要かどうかわからない場合はどうしたらよいですか?
YDCにお尋ね下さい。問合せをしたら費用が発生するということはありません。
再生医療の書類作成・申請・コンサルティング
薬事法ドットコム
全国の医師・歯科医のみなさまへ
再生医療申請の書類制作時間を圧縮。最短距離で申請をサポートいたします
お電話でもご相談いただけます
Tel. 03-6274-8781
